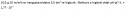Toplista

- betöltés...
Ha szívesen korrepetálnál, hozd létre magántanár profilodat itt.
Ha diák vagy és korrepetálásra van szükséged, akkor regisztrálj be és írd meg itt, hogy milyen tantárgyban!
PH, elektrolit, egyensúly - 216
 petoszilvi
kérdése
petoszilvi
kérdése
342
Csatoltam képet.
Jelenleg 1 felhasználó nézi ezt a kérdést.
0
Felsőoktatás / Kémia
Válaszok
1 kazah
megoldása
kazah
megoldása
`M_(HCOOH)` = 46 `g/(mol)`
`HCOOH` `Leftrightarrow` `HCOO^-` + `H^+`
100 g oldatban van 20 g hangyasav
10 g oldatban van `10/100*20` = 2 g hangyasav
Hígítjuk 5 `dm^3`-re
5 `dm^3` oldatban van 2 g hangyasav
1 `dm^3` oldatban van `1/5*2` = 0,4 g hangyasav, ami `0.4/46` = `8.7*10^(-3)` mol
Kiindulás: `8.7*10^(-3)` mol hangyasav
Átalakul: x mol hangyasav
Egyensúlyban: `8.7*10^(-3)`-x mol hangyasav; `8.7*10^(-3)` mol formiátion; `8.7*10^(-3)` mol hidrogénion.
`K_s` = `([HCOO^-]*[H^+])/([HCOOH])` = `x^2/((8.7*10^(-3)-x)` = `1.77*10^(-4)`
x = `1.15*10^(-3)` = `[H^+]`
pH = `-lg[H^+]` = -lg`1.15*10^(-3)` = 2,94
Az oldat pH-ja 2,94.
0
- Még nem érkezett komment!