Toplista

- betöltés...
Ha szívesen korrepetálnál, hozd létre magántanár profilodat itt.
Ha diák vagy és korrepetálásra van szükséged, akkor regisztrálj be és írd meg itt, hogy milyen tantárgyban!
Kémia feladatlap
 kira0111
{ Matematikus } kérdése
kira0111
{ Matematikus } kérdése
394
Sziasztok! Valaki tudna vele segíteni? Már egy-egy feladat is jó lenne
Jelenleg 1 felhasználó nézi ezt a kérdést.
0
Középiskola / Kémia
Válaszok
2 kazah
válasza
kazah
válasza
3.
`C_xH_yCl_z`
100 g vegyületben van
51,9 g szén, ez `51.9/12`= 4,325 mol
38,4 g klór, ez `38.4/35.5` = 1,0817 mol
A maradék hidrogén, az 100-(51,9+38,4) = 9,7 g, az pedig 9,7 mol
A mólarányok: (elosztjuk a klóréval, hátha csak egy van benne):
C:Cl:H = 4:1:9
A keresett vegyület összegképlete `C_4H_9Cl`
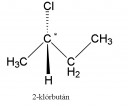
A vegyület királis, tehát tartalmaz egy szénatomot, amihez különböző funkciós csoportok kapcsolódnak. (R vagy S-2-klórbután)
(Ábra)
`C_xH_yCl_z`
100 g vegyületben van
51,9 g szén, ez `51.9/12`= 4,325 mol
38,4 g klór, ez `38.4/35.5` = 1,0817 mol
A maradék hidrogén, az 100-(51,9+38,4) = 9,7 g, az pedig 9,7 mol
A mólarányok: (elosztjuk a klóréval, hátha csak egy van benne):
C:Cl:H = 4:1:9
A keresett vegyület összegképlete `C_4H_9Cl`
A vegyület királis, tehát tartalmaz egy szénatomot, amihez különböző funkciós csoportok kapcsolódnak. (R vagy S-2-klórbután)
(Ábra)
0
- Még nem érkezett komment!
 kazah
válasza
kazah
válasza
2.
100 `dm^3` normálállapotú elegy az `100/22.41` = 4,462 mol
`CH_4` + 2 `O_2` `rightarrow` `CO_2` + 2 `H_2O`
`C_3H_8` + 7 `O_2` `rightarrow` 3 `CO_2` + 4 `H_2O`
Az elegy tartalmaz x mol propánt és 4,462-x mol metánt.
Az égéshő az ebben az esetben a reakcióhő, amit úgy számolunk ki, hogy
a keletkezett anyagok képződéshője - a kiindulási anyagok képződéshője (a sztöchiometriai számok figyelembevételével). Elemek képződéshője 0.
`Q_m` = `[2*(-241.8)+(-394)-(-74.9)]*(4.462-x)` = `802.7*(4.462-x)` kJ (a felszabaduló hő miatt legyen pozitív, a teljesnél is.)
`Q_p` = `[4*(-241.8)+3*(-394)-(-104)]*x` = 2045,2x kJ
A teljes felszabaduló hőmennyiség 6500 kJ.
`802.7*(4.462-x)` + `2045.2*x` = 6500
x = 2,349
4,462 mol elegyben van 2,349 mol propán
100 mol elegyben van `100/4.462*2.349` = 52,64 mol propán.
A gázelegy 52,64 mol% propánt és 100-52,64= 47,36 mol% metánt tartalmaz.
Azért számold át.
100 `dm^3` normálállapotú elegy az `100/22.41` = 4,462 mol
`CH_4` + 2 `O_2` `rightarrow` `CO_2` + 2 `H_2O`
`C_3H_8` + 7 `O_2` `rightarrow` 3 `CO_2` + 4 `H_2O`
Az elegy tartalmaz x mol propánt és 4,462-x mol metánt.
Az égéshő az ebben az esetben a reakcióhő, amit úgy számolunk ki, hogy
a keletkezett anyagok képződéshője - a kiindulási anyagok képződéshője (a sztöchiometriai számok figyelembevételével). Elemek képződéshője 0.
`Q_m` = `[2*(-241.8)+(-394)-(-74.9)]*(4.462-x)` = `802.7*(4.462-x)` kJ (a felszabaduló hő miatt legyen pozitív, a teljesnél is.)
`Q_p` = `[4*(-241.8)+3*(-394)-(-104)]*x` = 2045,2x kJ
A teljes felszabaduló hőmennyiség 6500 kJ.
`802.7*(4.462-x)` + `2045.2*x` = 6500
x = 2,349
4,462 mol elegyben van 2,349 mol propán
100 mol elegyben van `100/4.462*2.349` = 52,64 mol propán.
A gázelegy 52,64 mol% propánt és 100-52,64= 47,36 mol% metánt tartalmaz.
Azért számold át.
0
- Még nem érkezett komment!