Toplista

- betöltés...
Ha szívesen korrepetálnál, hozd létre magántanár profilodat itt.
Ha diák vagy és korrepetálásra van szükséged, akkor regisztrálj be és írd meg itt, hogy milyen tantárgyban!
Help! Nem megy a kémia!
 Nemmegyakemia
kérdése
Nemmegyakemia
kérdése
312
Holnapra kell csinálni kémia házit a munkafüzetben. Ha valaki segít annak nagyon köszönöm!
Jelenleg 1 felhasználó nézi ezt a kérdést.
kémia, munkafüzet
kémia, munkafüzet
0
Középiskola / Kémia
Válaszok
2 aladintszigi
válasza
aladintszigi
válasza
1.
Jó a +16, csak legyen mögötte mértékegység (+16 kJ/mol)
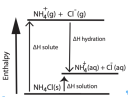
Mellékeltem egy diagramot, amely összefoglalja miért.
∆H solute: oldáshoz szükséges hő (végsősoron rácsenergia)
∆H hydration: hidratiációs hő
Állandó nyomáson ezek a reakcióhőnek (hő jellegű mennyiségnek) feleltethetők meg.
Tehát a magyarázat, hogy pozitív a reakcióhő, mivel az oldáshő értéke nagyobb, mint a hidratációs hő értéke. Tehát több energia kell ahhoz, hogy az ionok szilárd fázisból folyadékfázisba menjenek át, mint amennyit az ionok szolvatációja (a vízmolekulák dipólusként körülveszik) kompenzálja.
Emiatt a környezettől vesz el hőt (energiát). Emiatt endoterm az oldódás.
Ha melegítjük az oldatot, akkor egyrészt gyorsabban fog oldódni, illetve az oldhatósága is nőni fog. Nem teljesen triviális, hogy miért fog több oldatfázisba kerülni (pláne mivel a diagram állandó hőmérsékletre vonatkozik). Általában magasabb hőmérsékleten a nagyobb hőmozgás miatt egyszerűen másként áll be az egyensúly (kisebb összetartó erő a rácsban), ami kedvez az oldódásnak.
Jó a +16, csak legyen mögötte mértékegység (+16 kJ/mol)
Mellékeltem egy diagramot, amely összefoglalja miért.
∆H solute: oldáshoz szükséges hő (végsősoron rácsenergia)
∆H hydration: hidratiációs hő
Állandó nyomáson ezek a reakcióhőnek (hő jellegű mennyiségnek) feleltethetők meg.
Tehát a magyarázat, hogy pozitív a reakcióhő, mivel az oldáshő értéke nagyobb, mint a hidratációs hő értéke. Tehát több energia kell ahhoz, hogy az ionok szilárd fázisból folyadékfázisba menjenek át, mint amennyit az ionok szolvatációja (a vízmolekulák dipólusként körülveszik) kompenzálja.
Emiatt a környezettől vesz el hőt (energiát). Emiatt endoterm az oldódás.
Ha melegítjük az oldatot, akkor egyrészt gyorsabban fog oldódni, illetve az oldhatósága is nőni fog. Nem teljesen triviális, hogy miért fog több oldatfázisba kerülni (pláne mivel a diagram állandó hőmérsékletre vonatkozik). Általában magasabb hőmérsékleten a nagyobb hőmozgás miatt egyszerűen másként áll be az egyensúly (kisebb összetartó erő a rácsban), ami kedvez az oldódásnak.
0
- Még nem érkezett komment!
 aladintszigi
válasza
aladintszigi
válasza
Ha az olajos fázisban lévő szódabikarbónához (ez lesz alul) ételecetet csepegtetünk bele, akkor mivel a víz és az olajos fázis egymással nem elegyedik, emiatt apró cseppek formájában a víz szétválik az olajon belül. Mivel a víz sűrűsége nagyobb, emiatt lassan cseppekben lesüllyed a pohár aljára. Itt azonban találkozik a szódabikarbónával, ami miatt a vízcseppek környékén heves buborékfejlődés indul. Mivel az olaj viszkozitása nagyobb, emiatt a buborékok nem az olajon keresztül távoznak, hanem a vízcseppeket “feltolják” magukkal az olajon belül. (Ez az olaj mennyiségétől, és több paramétertől is függ)
(((Igen látványos kísérlet, ha meg van színezve a víz)))
4:
víz: konyhasó, cukor, ammónia, nátrium-hidroxid,
benzin: zsír, oxigén
Nem oldódik: homok, gyémánt
Az oldhatóság a polaritástól függ. Poláris anyagok (ionrácsos stb.) poláris oldószerben (pl. Vízben, metanolban stb.) oldódnak jól.
Apoláris anyagok (pl. Zsírok) apoláris oldószerben oldódnak jól (kőolaj frakciók; hexán, toluol)
Bizonyos anyagok egyikben sem oldódnak, mivel túl erős összetartó erő van köztük (gyémánt, szilícium-dioxid)
(((Igen látványos kísérlet, ha meg van színezve a víz)))
4:
víz: konyhasó, cukor, ammónia, nátrium-hidroxid,
benzin: zsír, oxigén
Nem oldódik: homok, gyémánt
Az oldhatóság a polaritástól függ. Poláris anyagok (ionrácsos stb.) poláris oldószerben (pl. Vízben, metanolban stb.) oldódnak jól.
Apoláris anyagok (pl. Zsírok) apoláris oldószerben oldódnak jól (kőolaj frakciók; hexán, toluol)
Bizonyos anyagok egyikben sem oldódnak, mivel túl erős összetartó erő van köztük (gyémánt, szilícium-dioxid)
0
- Még nem érkezett komment!