Toplista

- betöltés...
Ha szívesen korrepetálnál, hozd létre magántanár profilodat itt.
Ha diák vagy és korrepetálásra van szükséged, akkor regisztrálj be és írd meg itt, hogy milyen tantárgyban!
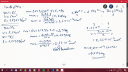
Egy lombikba bemérünk 5,00 cm3 térfogatú 8,00 tömeg%-os nátrium-foszfát (Na3PO4) oldatot, majd ehhez hozzámérünk 2,50 cm3 térfogatú, 18,0 tömegszázalékos bárium-klorid (BaCl2) oldatot.
 java.lang.Object
{ Kérdező } kérdése
java.lang.Object
{ Kérdező } kérdése
424
Egy lombikba bemérünk 5,00 cm3 térfogatú 8,00 tömeg%-os nátrium-foszfát (Na3PO4) oldatot, majd ehhez hozzámérünk 2,50 cm3 térfogatú, 18,0 tömegszázalékos bárium-klorid (BaCl2) oldatot. Számítsa ki, hogy intenzív keverés után, hány gramm bárium-foszfát (Ba3(PO4)2) csapadék keletkezett az oldatban! 3 Ba2+ + 2 PO4 3- = Ba3(PO4)2 ; Mr(Na3PO4)=163,94; Mr(BaCl2)=208,25; Mr(Ba3(PO4)2)=601,96; ρ(Na3PO4-oldat)=1,0961 g/cm3 ; ρ(BaCl2-oldat)=1,1793 g/cm3 ; ρ(H2O)=0,9975 g/cm3 ; (Az eredményt négy értékes jegyre adja meg!)
Válasz: 0,5113 gramm
Odáig jutottam, hogy kijött, hogy hány mol NaPO4 és BaCl2 a kiindulási oldatokban de nem tudok rájönni ebből, hogy jutok el a végső megoldásig. (Lehet sehogy )
)
Előre is köszi a segítséget!
Válasz: 0,5113 gramm
Odáig jutottam, hogy kijött, hogy hány mol NaPO4 és BaCl2 a kiindulási oldatokban de nem tudok rájönni ebből, hogy jutok el a végső megoldásig. (Lehet sehogy
 )
)Előre is köszi a segítséget!
Jelenleg 1 felhasználó nézi ezt a kérdést.
0
Felsőoktatás / Kémia