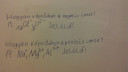Toplista

- betöltés...
Ha szívesen korrepetálnál, hozd létre magántanár profilodat itt.
Ha diák vagy és korrepetálásra van szükséged, akkor regisztrálj be és írd meg itt, hogy milyen tantárgyban!
Kémia-oxidálódás, redukálódás, ionok
 Annapanka
kérdése
Annapanka
kérdése
1011
Nem értem a kémiát. Nem tudom, hogy hogyan kell ezeket levezetni:
Hogyan képződnek a negatív ionok?
₁₇Cl-
₈O²-
Mi oxidálódott, mi redukálódott? (Először rendeznem kellene az egyenletet, utána ionosan leírnom)
Na+Cl₂-->
Mg+O₂-->
Nagyon megköszönném ha valaki tudna segíteni!
Hogyan képződnek a negatív ionok?
₁₇Cl-
₈O²-
Mi oxidálódott, mi redukálódott? (Először rendeznem kellene az egyenletet, utána ionosan leírnom)
Na+Cl₂-->
Mg+O₂-->
Nagyon megköszönném ha valaki tudna segíteni!
Jelenleg 1 felhasználó nézi ezt a kérdést.
kémia, egyenlet, 8. osztály
kémia, egyenlet, 8. osztály
0
Általános iskola / Kémia
Válaszok
6 rekademeter2
válasza
rekademeter2
válasza
A negatív ionok elektron felvétellel képződnek. ( a pozitívak elektron leadással)
Az oxidáció elektron leadást, amíg a redukció elektron felvételt jelent, így a Na oxidálódik, a Cl₂ redukálódik. Ugyanez a másodiknál is, a magnézium oxidálódik, az oxigén redukálódik.
Az oxidáció elektron leadást, amíg a redukció elektron felvételt jelent, így a Na oxidálódik, a Cl₂ redukálódik. Ugyanez a másodiknál is, a magnézium oxidálódik, az oxigén redukálódik.
0
- Még nem érkezett komment!
 rekademeter2
válasza
rekademeter2
válasza
Mindez úgy a legérthetőbb, hogyha az oxidációs számokat is figyelembe veszed. Tehát a nátrium és a klór oxidációs száma molekuláris állapotban nulla. Ezek egyesülésével NaCl keletkezik. Itt a nátrium oxidációs száma 1, a klóré -2. Tehát a nátrium elektront adott le, a klór elektront vett fel. Remélem tudtam segíteni. 

0
-
Annapanka: Köszönöm szépen! Sajnos még mindig nem teljesen világos. :( 8 éve 0
-
rekademeter2: Óó, hát akkor nem lenne jó tanár belőlem
 Szóval ugye az elektronok negatív előjelűek, ezért hogyha egy atom elektront vesz fel (redukció), akkor ő maga is negatív ion lesz
8 éve
0
Szóval ugye az elektronok negatív előjelűek, ezért hogyha egy atom elektront vesz fel (redukció), akkor ő maga is negatív ion lesz
8 éve
0
-
rekademeter2: Illetve ha egy atom elektront ad le, így válik belőle pozitív ion 8 éve 0
-
rekademeter2: Nyugodtan kérdezz ha nem világos, próbálok segíteni, csak nekem is nehéz érthetően elmagyarázni azokat amik mára már egyértelművé váltak
 8 éve
0
8 éve
0
-
Annapanka: Egy kicsit érthetőbb, de még mindig nem igazán értem, hogy a Mg+ egyenletrendezése hogyan jön ki így: Mg 2,8,2 12p+ 12e- ->-2e Mg 2+ 12p+ 10e- (Tudom, hogy ez pozitív, de csak ezt a példát tudtam leírni.) 8 éve 0
-
Annapanka: Illetve a pozitív még csak úgy dereng is, viszont a negatívé annyira sem. :/ 8 éve 0
-
rekademeter2: Tyű, hát nem igazán értem amit írtál, le tudnád fotózni a tankönyvben vagy a füzetedben ahol ezek le vannak írva? 8 éve 0
-
Annapanka: Igen, megpróbálom! 8 éve 0
 Annapanka
válasza
Annapanka
válasza
Nem sikerült a "kicsi válaszba" képet csatolnom.
Ez lenne a feladat, de mint mondtam nagyon nem értem. Így próbálkoztam például a Cl-ral.:
₁₇Cl- 2,8,7 -> e- ₁₇Cl- 2,8,8
. 17 e- 16 e-
. 17 p+ 17 p+
Cl atom Cl ion
Ez lenne a feladat, de mint mondtam nagyon nem értem. Így próbálkoztam például a Cl-ral.:
₁₇Cl- 2,8,7 -> e- ₁₇Cl- 2,8,8
. 17 e- 16 e-
. 17 p+ 17 p+
Cl atom Cl ion
Módosítva: 8 éve
0
- Még nem érkezett komment!
 rekademeter2
válasza
rekademeter2
válasza
Jajjj értem mááár, hogy mire gondolsz  A klórnál kis indexben a 17-es szám az itt most lényegtelen, a rendszámát jelöli, azaz, hogy hol helyezkedik el a periódusos rendszerben. A rendszámnak csak a protonok és neutronok kiszámításánál van jelentősége, az elektronoknak semmi köze hozzá. Szerintem itt csúszhattál el a dologban
A klórnál kis indexben a 17-es szám az itt most lényegtelen, a rendszámát jelöli, azaz, hogy hol helyezkedik el a periódusos rendszerben. A rendszámnak csak a protonok és neutronok kiszámításánál van jelentősége, az elektronoknak semmi köze hozzá. Szerintem itt csúszhattál el a dologban  Az, hogy egy ion hányszorosan lesz negatív, az dönti el hogy hanyadik főcsoportban (oszlopban) található. Tehát, ahhoz hogy a klór elérje a nemesgáz szerkezetet (nemesgázok az utolsó oszlopban vannak), egyetlen egy elektront tud csak felvenni. Ezt egyenletként felírva csak így lehet: Cl₂ + 2 e- = 2 Cl-. (Szóval egy mol klór 2 mol elektront tud felvenni, ugyanis itt klórmolekuláról beszélünk). Atomos szerkezetben (ami így leírva igazából nem létezik, csak azért mondom hogy megértsd) pl így nézne ki Cl + 1 e- = Cl-
Az, hogy egy ion hányszorosan lesz negatív, az dönti el hogy hanyadik főcsoportban (oszlopban) található. Tehát, ahhoz hogy a klór elérje a nemesgáz szerkezetet (nemesgázok az utolsó oszlopban vannak), egyetlen egy elektront tud csak felvenni. Ezt egyenletként felírva csak így lehet: Cl₂ + 2 e- = 2 Cl-. (Szóval egy mol klór 2 mol elektront tud felvenni, ugyanis itt klórmolekuláról beszélünk). Atomos szerkezetben (ami így leírva igazából nem létezik, csak azért mondom hogy megértsd) pl így nézne ki Cl + 1 e- = Cl-
 A klórnál kis indexben a 17-es szám az itt most lényegtelen, a rendszámát jelöli, azaz, hogy hol helyezkedik el a periódusos rendszerben. A rendszámnak csak a protonok és neutronok kiszámításánál van jelentősége, az elektronoknak semmi köze hozzá. Szerintem itt csúszhattál el a dologban
A klórnál kis indexben a 17-es szám az itt most lényegtelen, a rendszámát jelöli, azaz, hogy hol helyezkedik el a periódusos rendszerben. A rendszámnak csak a protonok és neutronok kiszámításánál van jelentősége, az elektronoknak semmi köze hozzá. Szerintem itt csúszhattál el a dologban  Az, hogy egy ion hányszorosan lesz negatív, az dönti el hogy hanyadik főcsoportban (oszlopban) található. Tehát, ahhoz hogy a klór elérje a nemesgáz szerkezetet (nemesgázok az utolsó oszlopban vannak), egyetlen egy elektront tud csak felvenni. Ezt egyenletként felírva csak így lehet: Cl₂ + 2 e- = 2 Cl-. (Szóval egy mol klór 2 mol elektront tud felvenni, ugyanis itt klórmolekuláról beszélünk). Atomos szerkezetben (ami így leírva igazából nem létezik, csak azért mondom hogy megértsd) pl így nézne ki Cl + 1 e- = Cl-
Az, hogy egy ion hányszorosan lesz negatív, az dönti el hogy hanyadik főcsoportban (oszlopban) található. Tehát, ahhoz hogy a klór elérje a nemesgáz szerkezetet (nemesgázok az utolsó oszlopban vannak), egyetlen egy elektront tud csak felvenni. Ezt egyenletként felírva csak így lehet: Cl₂ + 2 e- = 2 Cl-. (Szóval egy mol klór 2 mol elektront tud felvenni, ugyanis itt klórmolekuláról beszélünk). Atomos szerkezetben (ami így leírva igazából nem létezik, csak azért mondom hogy megértsd) pl így nézne ki Cl + 1 e- = Cl-
1
-
rekademeter2: Ennél jobban sajna tényleg nehéz elmagyarázni, főleg interneten, meg úgy, hogy nem nagyon tudom hogy eddig miket vettetek kémiából :/ 8 éve 0
-
Annapanka: Azt hiszem értem! Ha most két példát megoldok és feltöltöm, légyszíves lellenőriznéd, hogy jól csináltam-e meg? 8 éve 0
-
Annapanka: 8. osztályos vagyok, csak az a baj, hogy p 8 éve 0
-
Annapanka: *csak az a baj, hogy tavaly nem vettük végig, de a tanár most nem igazán veszi figyelembe és jóformán senki nem érti. (Lehet, hogy ez 7.-es anyag, csak tavaly nem vettük) 8 éve 0
-
Annapanka: Úgy látom kijelentkeztél, remélem nem baj ha elküldöm azt a két megoldásomat, hátha leellenőrzöd majd.
 8 éve
0
8 éve
0
 Annapanka
válasza
Annapanka
válasza
Remélem nem gond, hogy elküldtem a két megoldásomat. (:
Nagyon szépen köszönöm az eddigi válaszaidat is, sokat segítettél!
Nagyon szépen köszönöm az eddigi válaszaidat is, sokat segítettél!

0
- Még nem érkezett komment!
 rekademeter2
megoldása
rekademeter2
megoldása
Ne haragudj, igen tegnap már hamar kijelentkeztem, de most megnéztem a képeket amiket küldtél, és igen, viszonylag jól csináltad meg.  Mármint már látszik hogy érted miről van szó, ennek nagyon örülök.
Mármint már látszik hogy érted miről van szó, ennek nagyon örülök.  Ezen kívül csak az nem jó, hogy az elektronok száma nem egyezik meg a rendszámmal. Gondolom ezt azért nem tudtad mert nem vettétek, szerintem 9.-es anyag (meg a faktosok 11.-ben is tanulják), de megpróbálom elmagyarázni hátha megérted. Szóval a rendszámmal megegyezik az adott atomban lévő protonok száma/tömege. Tehát a klórban 17 proton van, ezt jól írtad fel.
Ezen kívül csak az nem jó, hogy az elektronok száma nem egyezik meg a rendszámmal. Gondolom ezt azért nem tudtad mert nem vettétek, szerintem 9.-es anyag (meg a faktosok 11.-ben is tanulják), de megpróbálom elmagyarázni hátha megérted. Szóval a rendszámmal megegyezik az adott atomban lévő protonok száma/tömege. Tehát a klórban 17 proton van, ezt jól írtad fel.  Viszont az elektronoknak olyan pici a tömege, hogy azt nem kell figyelembe venni. Tehát az nem stimmel a dologban, hogy a 17-es rendszámú klórban nem lehet 17 elektron.
Viszont az elektronoknak olyan pici a tömege, hogy azt nem kell figyelembe venni. Tehát az nem stimmel a dologban, hogy a 17-es rendszámú klórban nem lehet 17 elektron.
Továbbá hogy a reakció elején (a nyíl előtt), mivel ott atomos állapotban van az adott részecskénk, így nem lehet nála pozitív vagy negatív jel, csak a reakció után, érted? Tehát ha atomról beszélünk akkor simán Na-t kell írni, a reakció után, ahogy te is írtad, ionos szerkezetet kapunk és ott így kell felírni (amit jól is csináltál): Na+
 Mármint már látszik hogy érted miről van szó, ennek nagyon örülök.
Mármint már látszik hogy érted miről van szó, ennek nagyon örülök.  Ezen kívül csak az nem jó, hogy az elektronok száma nem egyezik meg a rendszámmal. Gondolom ezt azért nem tudtad mert nem vettétek, szerintem 9.-es anyag (meg a faktosok 11.-ben is tanulják), de megpróbálom elmagyarázni hátha megérted. Szóval a rendszámmal megegyezik az adott atomban lévő protonok száma/tömege. Tehát a klórban 17 proton van, ezt jól írtad fel.
Ezen kívül csak az nem jó, hogy az elektronok száma nem egyezik meg a rendszámmal. Gondolom ezt azért nem tudtad mert nem vettétek, szerintem 9.-es anyag (meg a faktosok 11.-ben is tanulják), de megpróbálom elmagyarázni hátha megérted. Szóval a rendszámmal megegyezik az adott atomban lévő protonok száma/tömege. Tehát a klórban 17 proton van, ezt jól írtad fel.  Viszont az elektronoknak olyan pici a tömege, hogy azt nem kell figyelembe venni. Tehát az nem stimmel a dologban, hogy a 17-es rendszámú klórban nem lehet 17 elektron.
Viszont az elektronoknak olyan pici a tömege, hogy azt nem kell figyelembe venni. Tehát az nem stimmel a dologban, hogy a 17-es rendszámú klórban nem lehet 17 elektron.Továbbá hogy a reakció elején (a nyíl előtt), mivel ott atomos állapotban van az adott részecskénk, így nem lehet nála pozitív vagy negatív jel, csak a reakció után, érted? Tehát ha atomról beszélünk akkor simán Na-t kell írni, a reakció után, ahogy te is írtad, ionos szerkezetet kapunk és ott így kell felírni (amit jól is csináltál): Na+
0
-
Annapanka: Így már teljesen világos, szerencsére a napokban sikerült ebből ötös dolgozatot írnom, neked hála.
 Még egyszer köszönöm!
Még egyszer köszönöm!  Ha a későbbiekben valami nem tiszta, kérdezhetlek majd?
8 éve
0
Ha a későbbiekben valami nem tiszta, kérdezhetlek majd?
8 éve
0
-
Annapanka: *Megint hamarabb küldtem el véletlen. Annyit szerettem volna hozzátenni még, hogyha nem lenne túl nagy kérés és idő. (,,Ha a későbbiekben valami nem tiszta, kérdezhetlek majd? Persze ha csak nem túl nagy kérés, és idő") 8 éve 0
-
rekademeter2: Nagyon örülök hogy jól sikerült, ügyi vagy
 És igen, persze, nyugodtan írhatsz ha bármi van!
8 éve
0
És igen, persze, nyugodtan írhatsz ha bármi van!
8 éve
0