Toplista

- betöltés...
Ha szívesen korrepetálnál, hozd létre magántanár profilodat itt.
Ha diák vagy és korrepetálásra van szükséged, akkor regisztrálj be és írd meg itt, hogy milyen tantárgyban!
Kémia feladat
 józsi092
kérdése
józsi092
kérdése
409
Egy telített szénhidrogén dihalogén-származéka 74,01 tömeg% halogént tartalmaz. A vegyület molekulája két kiralitás centrummal rendelkezik. Ha a vegyületet NaOH oldatban főzzük és a keletkezett oldatba klórgázt vezetünk a vizes oldat megbarnul. Benzint adva az oldathoz összerázás után a benzines fázis barna színű lesz.
a, Mi volt a halogénezett szénhidrogén összegképlete, konstitúciós képlete és neve?
b, A szerkezeti képletben jelölje csillaggal a kiralitás centrumokat! Hány optikai izomere van a vegyületnek és miért?
c, Melyik olefin halogénezésével állítható elő a telített diklórszármazék?
a, Mi volt a halogénezett szénhidrogén összegképlete, konstitúciós képlete és neve?
b, A szerkezeti képletben jelölje csillaggal a kiralitás centrumokat! Hány optikai izomere van a vegyületnek és miért?
c, Melyik olefin halogénezésével állítható elő a telített diklórszármazék?
Jelenleg 1 felhasználó nézi ezt a kérdést.
0
Középiskola / Kémia
Válaszok
1 kazah
megoldása
kazah
megoldása
A lúg hozzáadásával a halogéncsoportot lecseréljük hidroxilcsoportra és az oldatban ott lesznek a halogenidionok. Az, hogy a klórgáz leválasztja a halogént elemi állapotban, azt jelenti (a standardpotenciálok alapján), hogy a kérdéses halogén bróm vagy jód. Mivel mindkettő barna színű vízben, viszont benzinben a bróm változatlanul barna, a jód viszont lila. A kérdéses halogén tehát a bróm.
a,
A telített szénhidrogén dibrómszármazékának összegképlete: `C_xH_(2x)Br_2`, moláris tömege `12x+2x+2*80` = `14x+160` `g/(mol)`.
`14x+160` g vegyületben van 160 g bróm, ugyanakkor
100 g vegyületben van `100/(14x+160)*160` = 74,01 g bróm.
Az egyenletet megoldjuk, gyorsított eljárásban:
`x=(100*160/74.01-160)/14` = 4
A vegyület összegképlete tehát `C_4H_8Br_2`.
b,
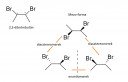
A szerkezeti képlete: Azt tudjuk, hogy két kiralitáscentrummal rendelkezik, ezért a nem szélső szénatomokhoz kapcsolódnak a brómatomok, továbbá két különbözőhöz. A két kiralitáscentrum négy enantiomert eredményezne, de a mezo-forma tükörképi párja önmaga, így csak három izomer van. Neve: 2,3-dibrómbután. A lehetséges szerkezetek az ábrán.
c, Hát elég érdekesen van a harmadik kérdés feltéve, hogy kapcsolódik-e a feladatohz, mert mint kiderült, dibrómszármazék a keresett vegyület.
Egyébként but-2-én az olefin, amiből elő lehet állítani a dihalogénszármazékot. A but-2-én is lehet cisz vagy transz, illetve kinetikai és termodinamikai kontrollal lehet szabályozni a három sztereoizomer arányát, de ez szerencsére már nem kérdés, hogy hogyan
a,
A telített szénhidrogén dibrómszármazékának összegképlete: `C_xH_(2x)Br_2`, moláris tömege `12x+2x+2*80` = `14x+160` `g/(mol)`.
`14x+160` g vegyületben van 160 g bróm, ugyanakkor
100 g vegyületben van `100/(14x+160)*160` = 74,01 g bróm.
Az egyenletet megoldjuk, gyorsított eljárásban:
`x=(100*160/74.01-160)/14` = 4
A vegyület összegképlete tehát `C_4H_8Br_2`.
b,
A szerkezeti képlete: Azt tudjuk, hogy két kiralitáscentrummal rendelkezik, ezért a nem szélső szénatomokhoz kapcsolódnak a brómatomok, továbbá két különbözőhöz. A két kiralitáscentrum négy enantiomert eredményezne, de a mezo-forma tükörképi párja önmaga, így csak három izomer van. Neve: 2,3-dibrómbután. A lehetséges szerkezetek az ábrán.
c, Hát elég érdekesen van a harmadik kérdés feltéve, hogy kapcsolódik-e a feladatohz, mert mint kiderült, dibrómszármazék a keresett vegyület.
Egyébként but-2-én az olefin, amiből elő lehet állítani a dihalogénszármazékot. A but-2-én is lehet cisz vagy transz, illetve kinetikai és termodinamikai kontrollal lehet szabályozni a három sztereoizomer arányát, de ez szerencsére már nem kérdés, hogy hogyan

1
-
józsi092: Köszönöm a gyors és részletes választ. 3 éve 0
-
kazah: Nagyon szívesen!
 3 éve
0
3 éve
0
-
bazsa990608: Atyám Kazah elolvastam amit írtál némelyik része elmenne nyelvtörőnek is
 Nagyon szép megoldás
Nagyon szép megoldás  3 éve
0
3 éve
0
-
kazah: Nahát, a kérdezőn kívül más is elolvassa? Akkor választékosabban fogalmazok legközelebb
 3 éve
0
3 éve
0
-
bazsa990608: Persze hogy el. Minden választ elszoktam olvasni. Hiszen mindíg lehet újat tanulni.
 3 éve
2
3 éve
2