Toplista

- betöltés...
Ha szívesen korrepetálnál, hozd létre magántanár profilodat itt.
Ha diák vagy és korrepetálásra van szükséged, akkor regisztrálj be és írd meg itt, hogy milyen tantárgyban!
Kémia feladat
 Flipflop
kérdése
Flipflop
kérdése
398
Csatoltam a kérdést. Köszönöm a segítséget.
Jelenleg 1 felhasználó nézi ezt a kérdést.
0
Középiskola / Kémia
Válaszok
1 kazah
válasza
kazah
válasza
`C_xH_y NO` + `x+y/4-1/2` `O_2` `rightarrow` x `CO_2` + `1/2` `N_2` + `y/2` `H_2O`
A nitrogénből érdemes kiindulni, 3,6 `dm^3` nitrogéngáz az adott körülmények között `3.6/24` = 0,15 mol; az egyenlet szerint is ennyi keletkezik.
0,3 mol amidhoz szükséges 1,725 mol oxigén
1 mol amidhoz szükséges `1/0.3*1.725` = 5,75 mol oxigén
I. `x+y/4-1/2` = 5,75
0,3 mol amidból keletkezik `52.8/44` = 1,2 mol `CO_2`
1 mol amidból keletkezik `1/0.3*1.2` = 4 mol `CO_2`
x = 4
0,3 mol amidból keletkezik `24.3/18` = 1,35 mol víz
1 mol amidból keletkezik `1/0.3*1.35` = 4,5 mol víz
`y/2` = 4,5
y = 9
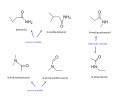
Az amid összegképlete: `C_4H_9NO`
Ha levonjuk a `C(=O)-NH_2` részt, marad az alkilcsoportra `C_3H_7 - `
Ez egy propilcsoport, ha primer-amidról van szó, lehet n-propil is izopropil-csoport.
Ha szekunder amid, akkor a nitrogénhez kapcsolódik egy metil és a C=O-hoz egy etilcsoport, vagy fordítva.
Ha tercier amid, akkor a nitrogénhez két metil vagy egy etil és egy metilcsoport kapcsolódik.
Összesen tehát 6 konstitúció lehetséges.
2,
`C_xH_yO_z` + n `O_2` `rightarrow` x `CO_2` + `y/2` `H_2O`
1 `dm^3` oldatban van 2 mol szénhidrát
8 `cm^3` oldatban van 16 mmol szénhidrát, ami 2,4 g
1 mol szénhidrát az `1/0.016*2.4` = 150 `g/(mol)` a moláris tömege.
Az összegképlete ez alapján `(CH_2O)_5` lesz, de azért számoljunk tovább.
16 mmol szénhidrát égetésekor keletkezik `3.52/44` = 80 mmol `CO_2`
x = `80/16` = 5
16 mmol szénhidrát elégetésekor keletkezett `1.44/18` = 80 mmol `H_2O`
`y/2` = 5 `rightarrow` y = 10
A moláris tömeg ismerete alapján az oxigén mennyisége 1 molban:
150-(5*12+10) = 80, ami éppen 5 oxigénatomot jelent.
Az összegképlet tehát `C_5H_(10)O_5`, valamelyik pentóz lesz.
3,
Ha csak a 21 db aminosav közül válogatunk, akkor feltételezzük, hogy nem a metionin és a cisztein, vagyis nincs benne kén.
Ezek után elindulunk úgy, hogy csak az amino és a karboxilcsoport van benne, mint funkciós csoport, így azt is feltételezzük, hogy a többi szén és hidrogén:
`H_2N-C_xH_y-COOH` + `(x+(y+3)/4-1-z)` `O_2` `rightarrow` x+1 `CO_2` + `1/2` `N_2` + `(y+3)/2` `H_2O`
A nitrogén mennyisége feleannyi, mint az aminosavé, így feltételezhetjük, hogy nincs több nitrogén a vegyületben.
Ha 0,5 mol aminosavból keletkezett 2 mol `CO_2`, akkor
1 mol aminosavból keletkezett 4 mol `CO_2`
x+1 = 4 `rightarrow` x = 3
Ha 0,5 mol aminosavból keletkezett 2,25 mol víz, akkor
1 mol aminosavból keletkezett 4,5 mol víz
`(y+3)/2` = 4,5 `rightarrow` y = 6
Oxigénre ellenőrizzük, hogy nem tartalmaz e más funkciós csoportot:
`x+(y+3)/4-1`+z=`2*2.375`
`3+(6+3)/4-1`+z = 4,75
4,25+z = 4,75
z = 0,5
A különbség adódhat mégegy oxigénből, esetleg hidroxilcsoport van az aminosavban.
Az összegképlet: `H_2N-C_3H_6O-COOH` vagy `C_4H_9NO_3`, az pedig a treonin.
A nitrogénből érdemes kiindulni, 3,6 `dm^3` nitrogéngáz az adott körülmények között `3.6/24` = 0,15 mol; az egyenlet szerint is ennyi keletkezik.
0,3 mol amidhoz szükséges 1,725 mol oxigén
1 mol amidhoz szükséges `1/0.3*1.725` = 5,75 mol oxigén
I. `x+y/4-1/2` = 5,75
0,3 mol amidból keletkezik `52.8/44` = 1,2 mol `CO_2`
1 mol amidból keletkezik `1/0.3*1.2` = 4 mol `CO_2`
x = 4
0,3 mol amidból keletkezik `24.3/18` = 1,35 mol víz
1 mol amidból keletkezik `1/0.3*1.35` = 4,5 mol víz
`y/2` = 4,5
y = 9
Az amid összegképlete: `C_4H_9NO`
Ha levonjuk a `C(=O)-NH_2` részt, marad az alkilcsoportra `C_3H_7 - `
Ez egy propilcsoport, ha primer-amidról van szó, lehet n-propil is izopropil-csoport.
Ha szekunder amid, akkor a nitrogénhez kapcsolódik egy metil és a C=O-hoz egy etilcsoport, vagy fordítva.
Ha tercier amid, akkor a nitrogénhez két metil vagy egy etil és egy metilcsoport kapcsolódik.
Összesen tehát 6 konstitúció lehetséges.
2,
`C_xH_yO_z` + n `O_2` `rightarrow` x `CO_2` + `y/2` `H_2O`
1 `dm^3` oldatban van 2 mol szénhidrát
8 `cm^3` oldatban van 16 mmol szénhidrát, ami 2,4 g
1 mol szénhidrát az `1/0.016*2.4` = 150 `g/(mol)` a moláris tömege.
Az összegképlete ez alapján `(CH_2O)_5` lesz, de azért számoljunk tovább.
16 mmol szénhidrát égetésekor keletkezik `3.52/44` = 80 mmol `CO_2`
x = `80/16` = 5
16 mmol szénhidrát elégetésekor keletkezett `1.44/18` = 80 mmol `H_2O`
`y/2` = 5 `rightarrow` y = 10
A moláris tömeg ismerete alapján az oxigén mennyisége 1 molban:
150-(5*12+10) = 80, ami éppen 5 oxigénatomot jelent.
Az összegképlet tehát `C_5H_(10)O_5`, valamelyik pentóz lesz.
3,
Ha csak a 21 db aminosav közül válogatunk, akkor feltételezzük, hogy nem a metionin és a cisztein, vagyis nincs benne kén.
Ezek után elindulunk úgy, hogy csak az amino és a karboxilcsoport van benne, mint funkciós csoport, így azt is feltételezzük, hogy a többi szén és hidrogén:
`H_2N-C_xH_y-COOH` + `(x+(y+3)/4-1-z)` `O_2` `rightarrow` x+1 `CO_2` + `1/2` `N_2` + `(y+3)/2` `H_2O`
A nitrogén mennyisége feleannyi, mint az aminosavé, így feltételezhetjük, hogy nincs több nitrogén a vegyületben.
Ha 0,5 mol aminosavból keletkezett 2 mol `CO_2`, akkor
1 mol aminosavból keletkezett 4 mol `CO_2`
x+1 = 4 `rightarrow` x = 3
Ha 0,5 mol aminosavból keletkezett 2,25 mol víz, akkor
1 mol aminosavból keletkezett 4,5 mol víz
`(y+3)/2` = 4,5 `rightarrow` y = 6
Oxigénre ellenőrizzük, hogy nem tartalmaz e más funkciós csoportot:
`x+(y+3)/4-1`+z=`2*2.375`
`3+(6+3)/4-1`+z = 4,75
4,25+z = 4,75
z = 0,5
A különbség adódhat mégegy oxigénből, esetleg hidroxilcsoport van az aminosavban.
Az összegképlet: `H_2N-C_3H_6O-COOH` vagy `C_4H_9NO_3`, az pedig a treonin.
0
-
Flipflop: Köszönöm szépen! Esetleg le tudná venni a megoldást?Köszönöm! 3 éve 0
-
Flipflop: Köszönöm szépen! Esetleg le tudná venni a megoldást?Köszönöm! 3 éve 0